包括18種第一批國家重點治理高值耗材......
1月12日,上海市藥監局、上海市醫保局、上海市衛健委三部門最新聯合發布了一則《上海市關于聯合推進醫療器械唯一標識系統全域試點工作方案》的通知(以下簡稱《通知》)。
《通知》中,三部門表示,為了進一步提升醫療器械全生命周期監管效能和醫療衛生管理效率,將全面推進醫療器械唯一標識系統全域試點工作。
按照要求,上海市將在首批醫療器械唯一標識(以下簡稱“唯一標識”)系統試點工作的基礎和經驗總結上,逐步拓寬試點品種和范圍。同時推進上海市醫療器械生產企業積極開展產品唯一標識工作,拓展唯一標識工作的參與度和覆蓋面。
不僅如此,三部門還強調,要選取部分重點品種,開展唯一標識與本市醫療器械統編代碼的映射(以下簡稱“兩碼映射”),探索拓展唯一標識在醫療、醫保、監管等領域的銜接應用。在此基礎上,逐步推進更多品種開展兩碼映射工作。
換句話說,上海市不僅要全面推進醫療器械唯一標識的全面落地,基于唯一標識還將進行更多的延伸和后續使用上的銜接工作。
文件的發布也就意味著,上海市第一批醫療器械“電子身份證”即將全面落地,此后上海市的醫療器械都將進行“實名制”管理。
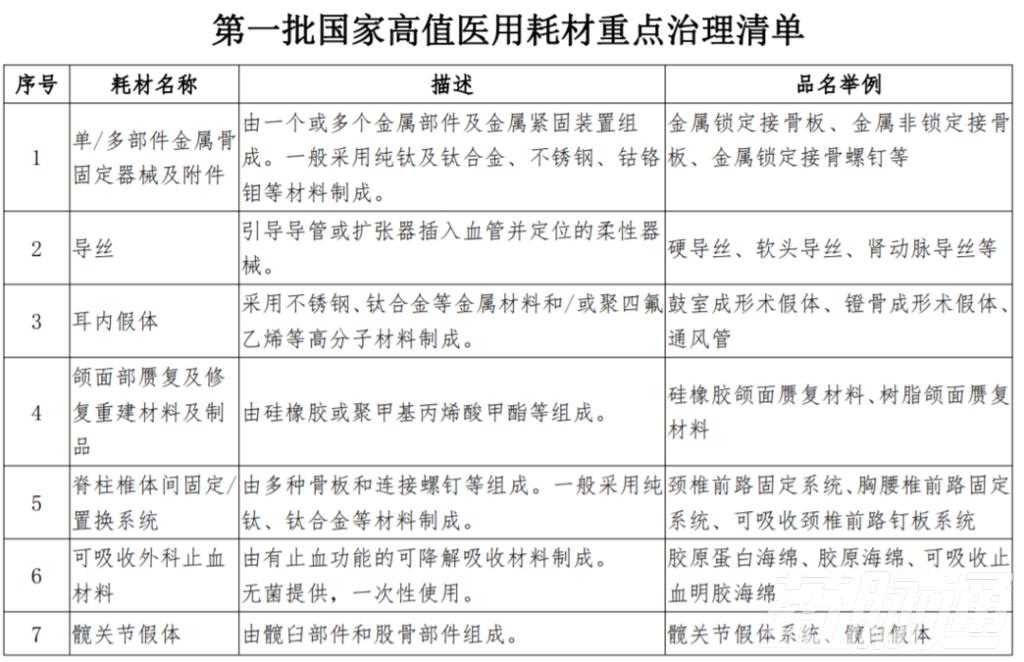
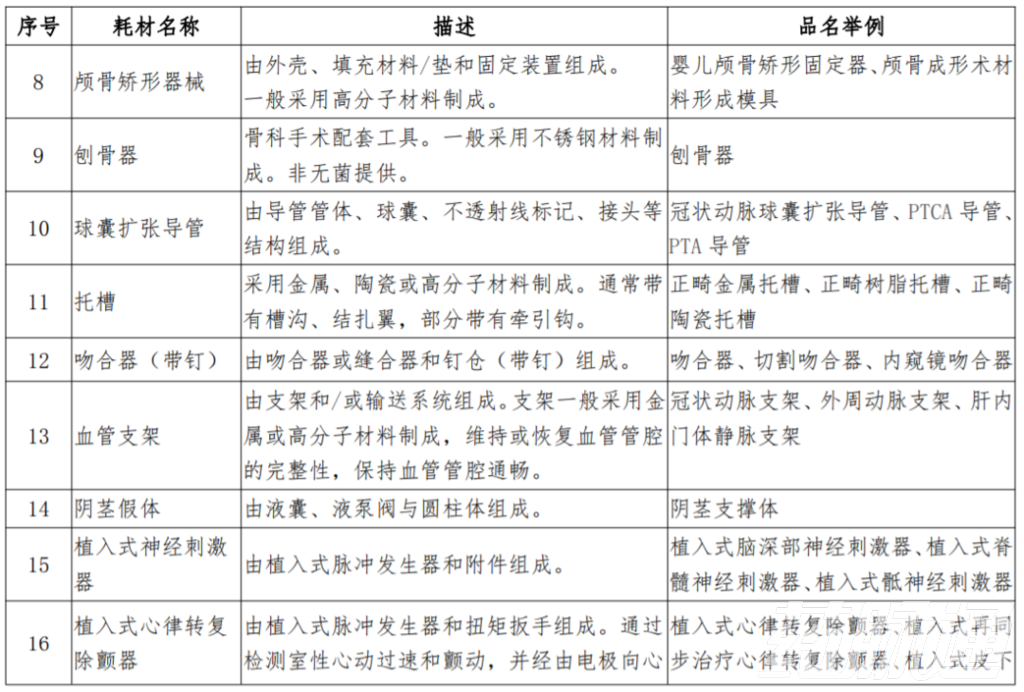
值得注意的是,在上海市公布的唯一標識試點品種中,三部門明確,除了關于深入推進試點做好第一批實施醫療器械唯一標識工作的公告》所列9大類69個品種之外,上海市還將把《第一批國家高值醫用耗材重點治理清單》中其他品種納入本市唯一標識試點范圍。
也就是說,除了國家藥監局公布的第一批試點品種之外,上海市還將對被納入第一批重點治理清單的18種高值醫用耗材“開刀”。
此外,在兩碼映射試點品種中,上海市將選取血管支架(分類編碼:13-07-02)、球囊擴張導管(分類編碼:03-13-06),植入式心臟起搏器(分類編碼:12-01-01)、植入式心臟起博電極導線(分類編碼:12-01-04)、植入式心律轉復除顫器(分類編碼:12-01-02)、植入式心臟除顫電極導線(分類編碼:12-01-05)、人工晶狀體(分類編碼:16-07-01)等7個重點品種開展兩碼映射試點。并且,在此基礎上,逐步推進更多品種開展兩碼映射工作。(篇幅限制,文末附第一批唯一標識清單)
事實上,就在2020年12月底,國家藥監局就會用國家衛健委、國家醫保局對第一批唯一標識實施工作進行了部署。
據國家醫保局相關負責人介紹,目前醫療器械唯一標識法規標準體系已經建成,全國范圍內第一批9大類69個品種將于2021年1月1日起正式實施唯一標識。
現階段,已經有多個省份開始逐漸部署試點。2020年12月末,湖南省就對2021年全省醫療器械唯一標識工作進行了部署。
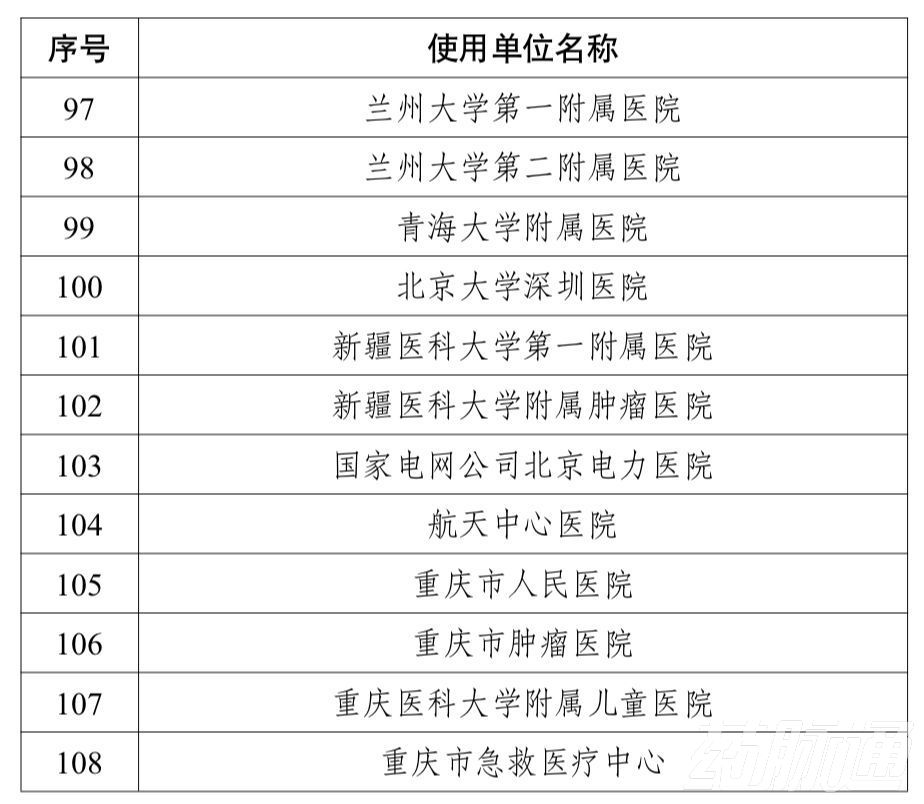
據湖南省表示,全省參與第一批實施醫療器械唯一標識(UDI)試點工作的單位包括生產企業8家、醫療機構2家,涉及品種21個。根據國家藥監局部署,湖南省第一批實施單位將于2021年1月1日起正式啟動醫療器械唯一標識(UDI)工作。
不僅如此,國家藥監局還表示,第二批唯一標識實施品種和政策也正在同步研究中,未來鼓勵企業將更多品種,特別是國家衛生健康委辦公廳印發的《第一批國家高值醫用耗材重點治理清單》中的產品納入試點范圍。
在對醫療器械行業監管的懲罰力度上,此前國務院更是強調,要對涉及質量安全的嚴重違法行為大幅提高罰款數額,對嚴重違法單位及責任人采取吊銷許可證、實行行業和市場禁入等嚴厲處罰,涉及犯罪的依法追究刑事責任。
醫療器械唯一標識上線后,將直接成為國家對于醫療器械的生產、經營以及使用監控的有力抓手。毫無疑問的是,透明化、可視化之下,無論是醫療器械廠商、代理商還是醫療機構,未來將受到的管控勢必也會更加嚴格......













 耦合劑智能供料器
耦合劑智能供料器 隔離透聲膜
隔離透聲膜 腔道用超聲耦合劑
腔道用超聲耦合劑 醫用無菌耦合劑
醫用無菌耦合劑